口罩CE認證事項及如何理解12號公告����,是多數(shù)口罩生產(chǎn)企業(yè)及貿(mào)易服務商關(guān)心的問題��。商務部為此撰文對12號公告熱點問題進行回應���,詳見正文��。
引言:口罩CE認證事項及如何理解12號公告��,是多數(shù)口罩生產(chǎn)企業(yè)及貿(mào)易服務商關(guān)心的問題�����。商務部為此撰文對12號公告熱點問題進行回應�,詳見正文�����。
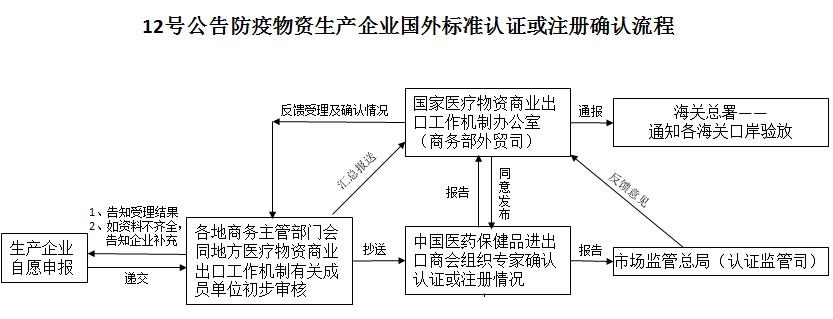
一���、商務部:關(guān)于12號公告熱點問題的回應
1.對4月26日前簽訂的非醫(yī)用口罩出口合同��,生產(chǎn)廠商是否需要列入醫(yī)保商會公布的取得國外標準認證或注冊的非醫(yī)用口罩生產(chǎn)企業(yè)清單中���?
答:不用。4月26日前簽訂的非醫(yī)用口罩出口合同按公告發(fā)布之前的方式執(zhí)行���,生產(chǎn)企業(yè)不必在醫(yī)保商會公布的取得國外標準認證或注冊的非醫(yī)用口罩生產(chǎn)企業(yè)清單內(nèi)����,但出口企業(yè)應當在報關(guān)時提交電子或書面的出口方和進口方共同聲明���。
2.針對新型冠狀病毒檢測試劑�、醫(yī)用口罩、醫(yī)用防護服�、呼吸機、紅外體溫計等5類醫(yī)療物資產(chǎn)品出口����,12號公告出臺后,5號公告是否繼續(xù)執(zhí)行�����?
答:5號公告繼續(xù)執(zhí)行���。12號公告是對5號公告的進一步完善和優(yōu)化�����,兩個公告同步執(zhí)行���。即如果5類醫(yī)療物資產(chǎn)品按中國質(zhì)量標準出口,需提供藥品監(jiān)督管理部門批準的醫(yī)療器械產(chǎn)品注冊證書����;如按國外質(zhì)量標準出口����,生產(chǎn)企業(yè)應為醫(yī)保商會公布的取得國外標準認證或注冊的生產(chǎn)企業(yè)清單中的企業(yè)��。
3.企業(yè)如何進入醫(yī)保商會公布的取得國外標準認證或注冊的防疫物資生產(chǎn)企業(yè)清單中��?
答:商務部已就此問題于4月25日專門下發(fā)《關(guān)于組織做好審核確認符合國外標準認證或注冊的防疫物資生產(chǎn)企業(yè)名單有關(guān)工作的通知》�,要求地方商務主管部門組織做好自愿申報和審核確認工作。該通知已在商務部網(wǎng)站公開發(fā)布�����。
(http://wms.mofcom.gov.cn/article/zcfb/g/202004/20200402959046.shtml)
4.對4月26日之后簽訂的非醫(yī)用口罩出口合同���,生產(chǎn)企業(yè)沒進入醫(yī)保商會公布的取得國外標準認證或注冊的非醫(yī)用口罩生產(chǎn)企業(yè)清單中,能否出口�����?
答:首先企業(yè)應明確出口的產(chǎn)品是符合中國標準還是國外標準����。如果出口方和進口方約定產(chǎn)品按國外標準出口,生產(chǎn)企業(yè)應當列入醫(yī)保商會公布的取得國外標準認證或注冊的非醫(yī)用口罩生產(chǎn)企業(yè)清單中����。如果出口方和進口方約定產(chǎn)品不是按國外標準出口�,且生產(chǎn)企業(yè)不在市場監(jiān)管總局提供的國內(nèi)市場查處的非醫(yī)用口罩質(zhì)量不合格產(chǎn)品和企業(yè)清單內(nèi)����,在企業(yè)提交共同聲明的情況下,相關(guān)產(chǎn)品可以出
口����。
5.醫(yī)療物資生產(chǎn)企業(yè)沒有國內(nèi)醫(yī)療器械產(chǎn)品注冊證書,有國外的CE��、FDA證書(在醫(yī)保商會公布的企業(yè)名單中)�����,但出口國沒有對應證書����,采購商合同和相關(guān)協(xié)議已約定接受國外質(zhì)量標準,出口如何處理��?
答:只要雙方約定接受國外標準即可����。相關(guān)標準不一定是進口國(地區(qū))的質(zhì)量標準�����。
二�、來自行業(yè)組織的回應:
1����、企業(yè)如何進入醫(yī)保商會公布的取得國外標準認證或注冊的防疫物資生產(chǎn)企業(yè)清單中?
答:根據(jù)4月26日國家醫(yī)療物資商業(yè)出口工作機制辦公室《關(guān)于組織做好審核確認符合國外標準認證或注冊的防疫物資生產(chǎn)企業(yè)名單有關(guān)工作的通知》要求���,各地方商務主管部門組織本地防疫物資生產(chǎn)企業(yè)自愿填報有關(guān)表格并提交相關(guān)證明材料�����。地方商務主管部門會同本地醫(yī)療物資商業(yè)出口工作機制有關(guān)成員單位初步審核后,以工作機制辦公室名義(本地商務主管部門代章)將匯總表(含電子版)統(tǒng)一報送至國家醫(yī)療物資商業(yè)出口工作機制辦公室(商務部外貿(mào)司)�,同時抄送我會。我會組織專家審核確認相關(guān)資質(zhì)并報商務部批準后動態(tài)更新名單���。
取得國外標準認證或注冊的非醫(yī)用口罩生產(chǎn)企業(yè)清單由地方商務主管部門初步審核后��,直接報送至國家醫(yī)療物資商業(yè)出口工作機制辦公室(商務部外貿(mào)司)�����,抄送醫(yī)保商會����。有任何疑問,企業(yè)可與當?shù)厣虅詹块T取得聯(lián)系�,咨詢具體申報材料要求及相關(guān)填報信息。
2�、企業(yè)資料上報有時限么?
從4月26日公告發(fā)布到4月29日�,每天地方商務主管部門可根據(jù)本地區(qū)企業(yè)申報情況,初步審核后���,報送國家醫(yī)療物資商業(yè)出口工作機制辦公室(商務部外貿(mào)司)�,抄送我會�����。自4月30日起�����,原則上每周報送一次����,地方商務部門上報截止時間為每周三17:00�����。
3��、清單發(fā)布的頻率是怎樣的�?
答:我會將在組織專家完成確認工作后��,將結(jié)果報送商務部��,并將根據(jù)商務部要求適時發(fā)布(通常為2-3天)���。
4. 企業(yè)如何知道是否通過�����?不合格原因是否可以反饋企業(yè)���?企業(yè)能否補交資料�����?
答:國家醫(yī)療物資商業(yè)出口工作機制辦公室會將結(jié)果通知地方商務主管部門,企業(yè)可向地方商務主管部門咨詢��。資料審核確認過程中��,如發(fā)現(xiàn)企業(yè)提交的資料不完整�,會反饋給地方商務主管部門,由地方商務主管部門通知企業(yè)補交資料�����。
5����、想進入名錄的話是否必須成為商會會員?
答:商會是配合政府主管部門開展的工作��,該項工作與企業(yè)是否成為商會會員無關(guān)����。
中國醫(yī)藥保健品進出口商會(以下簡稱醫(yī)保商會)受政府主管部門委托,組織行業(yè)專家基于國外藥品監(jiān)管部門提供或發(fā)布的信息�、經(jīng)授權(quán)標準認證機構(gòu)數(shù)據(jù)庫等資源,就防疫物資生產(chǎn)企業(yè)有關(guān)產(chǎn)品取得的國外標準認證或注冊情況進行核對確認����。此項工作是醫(yī)保商會為政府主管部門提供的專業(yè)性公共服務��,確認結(jié)果與申請企業(yè)是否為醫(yī)保商會會員無關(guān)����。
醫(yī)保商會致力于推動中國醫(yī)藥健康產(chǎn)業(yè)國際化發(fā)展�����,在抗擊疫情特殊時期���,將秉持辦會宗旨��,繼續(xù)以公正�����、高效�、務實的工作��,更好服務于我國醫(yī)藥健康企業(yè)和行業(yè)健康發(fā)展�����,更有效支持國際社會抗擊疫情���。
感謝大家對商會工作的關(guān)注�,歡迎各界對我們的工作進行監(jiān)督并提出寶貴意見�。我們將攜手為中國醫(yī)藥健康企業(yè)“走出去”貢獻更大的力量。
6�、外貿(mào)企業(yè)申請加入醫(yī)保商會公布的取得國外標準認證或注冊的企業(yè)清單有何要求?
答:清單公布的是取得國外標準認證或注冊的防疫物資生產(chǎn)企業(yè)����,屬于供貨企業(yè),外貿(mào)企業(yè)可以協(xié)助或提醒供應商申請加入�。
7、5號公告范圍內(nèi)的產(chǎn)品�����,已在國家藥監(jiān)局注冊�����,但不在12號公告里醫(yī)保商會的清單上����,可否正常出口?
答:兩個公告涉及的主體對象有所不同�,同步執(zhí)行��。其中12號公告是對5號公告的進一步完善和優(yōu)化�。即�����,5號公告針對的是五類醫(yī)療防疫物資的出口行為����,明確該類物資出口必須符合中國質(zhì)量標準要求,需提供藥監(jiān)部門出具的醫(yī)療器械注冊證��;對于專供出口的企業(yè)�����,包括海外代加工企業(yè)�����,通常是按照國外質(zhì)量標準要求進行生產(chǎn)的����,如未在我國獲得藥監(jiān)部門注冊認證,企業(yè)應取得國外標準認證或注冊���,并體現(xiàn)在我會網(wǎng)站公布的生產(chǎn)企業(yè)清單中�����。同時��,自4月26日起���,企業(yè)報關(guān)時還需要提交書面聲明,承諾產(chǎn)品符合進口國(地區(qū))質(zhì)量標準和安全要求�����。
標簽:口罩CE認證��、醫(yī)療器械CE認證