熱濕交換器是非常實用的醫(yī)療器械之一,近期�,藥監(jiān)總局發(fā)布《熱濕交換器注冊技術(shù)審查指導(dǎo)原則》,用于指導(dǎo)醫(yī)療器械注冊人注冊申報及醫(yī)療器械注冊審評人員審評審批���。
引言:熱濕交換器是非常實用的醫(yī)療器械之一���,近期�,藥監(jiān)總局發(fā)布《熱濕交換器注冊技術(shù)審查指導(dǎo)原則》��,用于指導(dǎo)醫(yī)療器械注冊人注冊申報及醫(yī)療器械注冊審評人員審評審批���。

熱濕交換器注冊技術(shù)審查指導(dǎo)原則
本指導(dǎo)原則旨在為申請人進(jìn)行熱濕交換器(HME)產(chǎn)品注冊申報提供技術(shù)指導(dǎo)��,同時也為藥品監(jiān)督管理部門對注冊申報資料的審評提供技術(shù)參考���。
本指導(dǎo)原則是對熱濕交換器產(chǎn)品注冊申報資料的一般要求,申請人應(yīng)依據(jù)具體產(chǎn)品的特性對注冊申報資料的內(nèi)容進(jìn)行充實和細(xì)化�,并依據(jù)具體產(chǎn)品的特性確定其中的具體內(nèi)容是否適用��,若不適用�,需具體闡述其理由及相應(yīng)的科學(xué)依據(jù)。
本指導(dǎo)原則是對申請人和審評人員的指導(dǎo)性文件����,但不包括注冊審批所涉及的行政事項,亦不作為法規(guī)強(qiáng)制執(zhí)行����,如果有能夠滿足相關(guān)法規(guī)要求的其他方法,也可以采用��,但是需要提供詳細(xì)的研究資料和驗證資料。應(yīng)在遵循相關(guān)法規(guī)和標(biāo)準(zhǔn)的前提下使用本指導(dǎo)原則�。
本指導(dǎo)原則是在現(xiàn)行法規(guī)和標(biāo)準(zhǔn)體系以及當(dāng)前認(rèn)知水平下制定的,隨著法規(guī)和標(biāo)準(zhǔn)的不斷完善�����,以及科學(xué)技術(shù)的不斷發(fā)展���,本指導(dǎo)原則相關(guān)內(nèi)容也將進(jìn)行適時的調(diào)整��。
一����、適用范圍
本指導(dǎo)原則適用于《醫(yī)療器械分類目錄》(國家食品藥品監(jiān)督管理總局公告2017第104號)中管理類別為Ⅱ類的熱濕交換器�,分類編碼為08-05-04(呼吸�、麻醉和急救器械-呼吸��、麻醉�����、急救設(shè)備輔助裝置-熱濕交換器)�。通常由儲水儲熱材料和殼體組成,包括一個進(jìn)氣口和一個出氣口,通過保留患者呼氣中部分水分和熱量����,并在吸氣過程中將其返回到呼吸道的器械。用于提高輸送給呼吸道的氣體中的水分含量和溫度��。
二���、技術(shù)審查要點
(一)產(chǎn)品名稱要求
產(chǎn)品名稱應(yīng)符合《醫(yī)療器械通用名稱命名規(guī)則》(國家食品藥品監(jiān)督管理總局令第19號)的要求���,可采用相關(guān)國家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)上的通用名稱��,或以產(chǎn)品結(jié)構(gòu)和適用范圍為依據(jù)命名�。如熱濕交換器、熱濕交換過濾器��。根據(jù)產(chǎn)品一次性使用或者滅菌情況�����,產(chǎn)品名稱中可帶有“一次性使用”或“無菌”字樣�����。
(二)產(chǎn)品的結(jié)構(gòu)和組成
產(chǎn)品通常由外殼�����、濾芯(如有)�����、熱濕交換介質(zhì)和接口等組成�。

圖1
1-機(jī)器端口;2-輔助端口���;3-外殼���;4-熱濕交換介質(zhì);5-患者端口
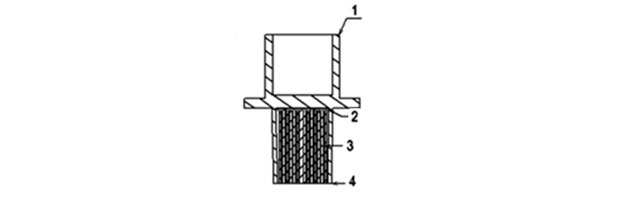
圖2
1-患者端口��;2-外殼��;3-熱濕交換介質(zhì)��;4 -機(jī)器端口
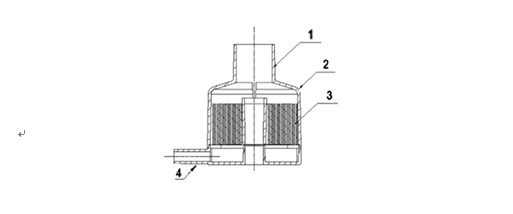
圖3
1-患者端口���;2-外殼�;3-熱濕交換介質(zhì);4-輔助端口
(三)產(chǎn)品工作原理
熱濕交換器是一種保溫保濕氣道管理工具��,可以將病人呼出氣體中的熱量和水分部分地儲存起來��,再利用這些熱量和水分對新進(jìn)入的氣體進(jìn)行加溫及濕化�。
呼氣時,來自病人的溫濕氣體進(jìn)入熱濕交換器的內(nèi)側(cè)面���,濕氣凝結(jié)��,同時釋放的熱量在熱濕交換介質(zhì)中得以保存����。吸氣時���,外部干燥的氣體進(jìn)入熱濕交換器��,在熱濕交換器內(nèi)得到濕化和溫?zé)?��,然后進(jìn)入肺內(nèi),如此往復(fù)循環(huán)�����,不斷利用呼氣中的熱度和濕度來溫?zé)岷蜐窕氲臍怏w�。
產(chǎn)品如聲稱具有過濾功能,應(yīng)說明過濾作用(如過濾微粒����、細(xì)菌及病毒過濾等)及其原理。
(四)注冊單元劃分的原則
注冊單元劃分參照《總局關(guān)于發(fā)布醫(yī)療器械注冊單元劃分指導(dǎo)原則的通告》(2017年第187號)�,著重考慮產(chǎn)品的技術(shù)原理、結(jié)構(gòu)組成���、性能指標(biāo)�����、適用范圍等因素��。
(五)產(chǎn)品適用的相關(guān)標(biāo)準(zhǔn)
表1 相關(guān)產(chǎn)品標(biāo)準(zhǔn)
標(biāo)準(zhǔn)編號 | 標(biāo)準(zhǔn)名稱 |
GB/T 191-2008 | 《包裝儲運圖示標(biāo)志》 |
GB/T 1962.1-2015 | 《注射器�����、注射針及其他醫(yī)療器械用6%(魯爾)圓錐接頭 第1部分:通用要求》 |
GB/T 2828.1-2012 | 《計數(shù)抽樣檢驗程序 第1部分:按接收質(zhì)量限(AQL)檢索的逐批檢驗抽樣計劃》 |
GB/T 14233.1-2008 | 《醫(yī)用輸液�、輸血��、注射器具檢驗方法 第1部分:化學(xué)分析方法》 |
GB/T 14233.2-2005 | 《醫(yī)用輸液���、輸血���、注射器具檢驗方法 第2部分:生物學(xué)試驗方法》 |
GB/T 16886.1-2011 | 《醫(yī)療器械生物學(xué)評價 第1部分:風(fēng)險管理過程中的評價與試驗》 |
GB/T 16886.5-2017 | 《醫(yī)療器械生物學(xué)評價 第5部分:體外細(xì)胞毒性試驗》 |
GB/T 16886.7-2015 | 《醫(yī)療器械生物學(xué)評價 第7部分:環(huán)氧乙烷滅菌殘留量》 |
GB/T 16886.10-2017 | 《醫(yī)療器械生物學(xué)評價 第10部分:刺激與皮膚致敏試驗》 |
YY/T 0313-2014 | 《醫(yī)用高分子產(chǎn)品 包裝和制造商提供信息的要求》 |
YY/T 0466.1-2016 | 《醫(yī)療器械 用于醫(yī)療器械標(biāo)簽�、標(biāo)記和提供信息的符號 第1部分:通用要求》 |
YY/T 0735.1-2009 | 《麻醉和呼吸設(shè)備 濕化人體呼吸氣體的熱濕交換器(HME) 第1部分:用于最小潮氣量為250mL的HME》 |
YY/T 0735.2-2010 | 《麻醉和呼吸設(shè)備 用于加濕人體呼吸氣體的熱濕交換器(HMEs) 第2部分:用于氣管切開術(shù)患者的250mL以上潮氣量的HMEs》 |
YY/T 1040.1-2015 | 《麻醉和呼吸設(shè)備 圓錐接頭 第1部分:錐頭與錐套》 |
YY/T 1040.2-2008 | 《麻醉和呼吸設(shè)備 圓錐接頭 第2部分:螺紋承重接頭》 |
注:本指導(dǎo)原則中標(biāo)準(zhǔn)適用最新版本����,下同。聲稱產(chǎn)品具有過濾功能的����,應(yīng)選用相應(yīng)適用的標(biāo)準(zhǔn)。
上述標(biāo)準(zhǔn)包括了注冊產(chǎn)品技術(shù)要求中通常涉及到的標(biāo)準(zhǔn)���。企業(yè)可根據(jù)產(chǎn)品的特點引用其他適用的國家�����、行業(yè)標(biāo)準(zhǔn)���。
產(chǎn)品適用及引用標(biāo)準(zhǔn)的審查可以分兩步來進(jìn)行。首先對引用標(biāo)準(zhǔn)的齊全性和適宜性進(jìn)行審查����,也就是在編寫產(chǎn)品技術(shù)要求時是否引用了與產(chǎn)品相關(guān)的國家標(biāo)準(zhǔn)��、行業(yè)標(biāo)準(zhǔn),以及引用是否準(zhǔn)確�����?����?梢酝ㄟ^查閱其提交的研究資料��,對是否引用了相關(guān)標(biāo)準(zhǔn)�,以及所引用的標(biāo)準(zhǔn)是否適宜來進(jìn)行審查。此時���,應(yīng)注意標(biāo)準(zhǔn)編號�����、標(biāo)準(zhǔn)名稱是否完整規(guī)范�,年代號是否有效���。
其次對引用標(biāo)準(zhǔn)的采納情況進(jìn)行審查��。即所引用的標(biāo)準(zhǔn)中的條款要求��,是否在產(chǎn)品技術(shù)要求中進(jìn)行了實質(zhì)性的條款引用�����。這種引用通常采用兩種方式�,文字表述繁多內(nèi)容復(fù)雜的可以直接引用標(biāo)準(zhǔn)及條文號,比較簡單的也可以直接引述具體要求�。
如有新版強(qiáng)制性國家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)發(fā)布實施�����,產(chǎn)品性能指標(biāo)等要求應(yīng)執(zhí)行最新版本的國家標(biāo)準(zhǔn)�、行業(yè)標(biāo)準(zhǔn)。
(六)產(chǎn)品的適用范圍/禁忌癥
熱濕交換器用于提高輸送給呼吸道的氣體中的水分含量和溫度��。
禁忌癥:
1.呼吸道有大量泡沫或黏稠分泌物�����、脫水�����、咳血癥或呼吸道損傷的病人禁用。
2.對于嚴(yán)重肺功能不全等不能耐受通路阻力增加者禁用��。
3.對本產(chǎn)品材料過敏者禁用�。
(七)產(chǎn)品的主要風(fēng)險
1.風(fēng)險分析方法
1.1在對風(fēng)險的判定及分析中,要考慮合理的可預(yù)見的情況�����,它們包括:正常使用條件下��;非正常使用條件下��;
1.2風(fēng)險判定及分析應(yīng)包括:對于患者的危險(源)��;對于操作者的危險(源)���;對于環(huán)境的危險(源);
1.3風(fēng)險形成的初始原因應(yīng)包括:人為因素包括不合理的操作����;產(chǎn)品結(jié)構(gòu)、原材料�����、綜合危險(源);環(huán)境條件��;
1.4風(fēng)險判定及分析考慮的問題包括:產(chǎn)品原材料生物學(xué)危險(源)��;產(chǎn)品質(zhì)量是否會導(dǎo)致使用中出現(xiàn)不正常結(jié)果�;操作信息,包括警示性語言�、注意事項以及使用方法的準(zhǔn)確性;使用可能存在的危險(源)等�����。
2.風(fēng)險分析清單
熱濕交換器產(chǎn)品的風(fēng)險管理報告應(yīng)符合YY/T 0316-2016《醫(yī)療器械風(fēng)險管理對醫(yī)療器械的應(yīng)用》的有關(guān)要求����,審查要點包括:
2.1產(chǎn)品安全性特征判定是否準(zhǔn)確(依據(jù)YY/T 0316-2016附錄C);
2.2危險(源)分析是否全面(依據(jù)YY/T 0316-2016附錄E)�����;
2.3風(fēng)險可接收準(zhǔn)則���,降低風(fēng)險的措施及采取措施后風(fēng)險的可接收程度����,是否有新的風(fēng)險產(chǎn)生。
根據(jù)YY/T 0316-2016《醫(yī)療器械 風(fēng)險管理對醫(yī)療器械的應(yīng)用》附錄E對“熱濕交換器產(chǎn)品”已知或可預(yù)見的風(fēng)險進(jìn)行判定�,產(chǎn)品在進(jìn)行風(fēng)險分析時至少應(yīng)包括以下的主要危險(源),企業(yè)還應(yīng)根據(jù)自身產(chǎn)品特點確定其他危險(源)�。針對產(chǎn)品的各項風(fēng)險,企業(yè)應(yīng)采取應(yīng)對措施��,確保風(fēng)險降到可接受的程度����。
表2 產(chǎn)品主要危險(源)
危險(源)的分類 | 危險(源)的形成因素 | 可能的后果 |
生物學(xué)危險(源) | 生物污染 | 生產(chǎn)環(huán)境控制不好����。滅菌操作不嚴(yán)格。包裝破損��。使用時操作不正規(guī)�。 | 產(chǎn)品帶菌,引起患者使用時感染��。 |
生物不相容性 | 增塑劑����、加工助劑、 環(huán)氧乙烷殘留量超標(biāo) | 產(chǎn)生細(xì)胞毒性、致敏反應(yīng)���、急性或慢性毒性���。 |
不正確的配方(化學(xué)成分) | 未按照工藝要求配料。小分子物質(zhì)殘留量過大���。 | 造成毒性危害�����。 |
加工工藝 | 加工工藝控制不嚴(yán)格���,后處理工藝控制不嚴(yán)格。 | 引入有害物質(zhì)�,引起患者感染或造成毒性危害。 |
再感染和/或交叉感染 | 使用不當(dāng)��、標(biāo)識不清�����。 | 引起局部或者交叉感染��。 |
環(huán)境危險(源) | 儲存或運行偏離預(yù)定的環(huán)境條件 | 儲運條件(如溫度、濕度)不符合要求���。 | 產(chǎn)品老化�����。 無菌有效期縮短���。 |
意外的機(jī)械破壞 | 儲運、使用過程中發(fā)生意外的機(jī)械性破壞����。 | 產(chǎn)品使用性能無法得到保證。 |
由于廢物和/或醫(yī)療器械處置的污染 | 使用后的產(chǎn)品沒有按照要求集中銷毀�。 | 造成環(huán)境污染或者細(xì)菌的交叉感染����。 |
與醫(yī)療器械使用有關(guān)的危險(源) | 不適當(dāng)?shù)臉?biāo)記 | 標(biāo)記不清晰、錯誤���、 沒有按照要求進(jìn)行標(biāo)記�����。 | 錯誤使用����。 儲存錯誤。 產(chǎn)品辨別錯誤����。 |
不適當(dāng)?shù)牟僮髡f明,如: 與其他器械配合使用不適當(dāng)�;偏離使用說明;說明書關(guān)于使用說明不全面 | 包裝破損無法識別��。 操作要點不突出����。 | 無法保證使用安全性。 導(dǎo)致操作失誤�����。 |
由不熟練/未經(jīng)培訓(xùn)的人員使用 | 操作不熟練��、操作失誤��。 | 導(dǎo)致延誤或不正確治療��。 |
合理可預(yù)見的誤用 | 規(guī)格型號選用錯誤。 | 導(dǎo)致無法達(dá)到滿意的效果��。 |
對一次性使用醫(yī)療器械很可能再次使用的危險(源)警告不適當(dāng) | 造成重復(fù)使用����。 | 交叉感染。 |
不適當(dāng)不合適或過于復(fù)雜的使用者接口 | 違反或縮減說明書���、程序等 | 操作方法�����、注意事項���、儲存方法、警示事項等表述不清�。 | 重復(fù)使用引起感染。 沒有集中銷毀造成環(huán)境污染等���。 |
功能性失效、老化引起的危險(源) | 對醫(yī)療器械壽命終止缺少適當(dāng)?shù)臎Q定 | 沒有標(biāo)識產(chǎn)品有效期��。 | 超出滅菌有效期的產(chǎn)品被使用�,造成細(xì)菌感染��。 |
不適當(dāng)?shù)陌b(醫(yī)療器械的污染和/或變質(zhì)) | 沒有進(jìn)行包裝確認(rèn)���。 | 不能確保產(chǎn)品無菌,從而導(dǎo)致出現(xiàn)細(xì)菌感染��。 |
再次使用和/或不適當(dāng)?shù)脑俅问褂?/span> | 產(chǎn)品標(biāo)識沒有明確只限一次性使用����。 | 出現(xiàn)細(xì)菌感染、交叉感染以及粘膜損傷等現(xiàn)象�����。 |
(八)產(chǎn)品的研究要求
1.產(chǎn)品性能研究
應(yīng)詳述產(chǎn)品技術(shù)要求中主要性能指標(biāo)及檢驗方法的確定依據(jù)���,提供采用的原因及理論基礎(chǔ)���,提供涉及的研究性資料、文獻(xiàn)資料和標(biāo)準(zhǔn)文本��。如適用的國家標(biāo)準(zhǔn)�、行業(yè)標(biāo)準(zhǔn)中有不采納的條款,應(yīng)將不采納的條款及其理由予以闡明�。
應(yīng)研究的產(chǎn)品基本性能至少包括YY/T 0735.1-2009或YY/T 0735.2-2010規(guī)定的性能����。
對于聲稱產(chǎn)品具有過濾功能的����,企業(yè)應(yīng)提出相應(yīng)安全性、有效性的要求���。
潮氣量小于250mL的熱濕交換器�����,申請人應(yīng)確定評價方法或者參考YY/T 0735.1-2009或YY/T 0735.2-2010��,并調(diào)整試驗參數(shù)�����。
2.生物相容性研究
應(yīng)描述熱濕交換器與人體間接接觸部件的材料�,以及接觸的性質(zhì)和時間��,參照《關(guān)于印發(fā)醫(yī)療器械生物學(xué)評價和審評指南的通知》(國食藥監(jiān)械〔2007〕345號)�����、GB/T 16886.1-2011《醫(yī)療器械生物學(xué)評價 第1部分:風(fēng)險管理過程中的評價與試驗》的要求對其進(jìn)行生物相容性評價���。
3.滅菌工藝及潔凈控制工藝研究
3.1按GB 18278.1-2015《醫(yī)療保健品滅菌 濕熱 第1部分:醫(yī)療器械滅菌過程的開發(fā)�、確認(rèn)和常規(guī)控制要求》���、GB 18279.1-2015《醫(yī)療保健產(chǎn)品滅菌 環(huán)氧乙烷 第1部分:醫(yī)療器械滅菌過程的開發(fā)�、確認(rèn)和常規(guī)控制的要求》��、GB/T 18279.2-2015《醫(yī)療保健產(chǎn)品的滅菌 環(huán)氧乙烷 第2部分:GB 18279.1應(yīng)用指南》�����、GB 18280.1-2015《醫(yī)療器械保健產(chǎn)品滅菌 輻射 第1部分:醫(yī)療器械滅菌過程的開發(fā)�、確認(rèn)和常規(guī)控制要求》、GB 18280.2-2015《醫(yī)療保健產(chǎn)品滅菌 輻射 第2部分:建立滅菌劑量》�����、GB/T 18280.3-2015《醫(yī)療保健產(chǎn)品滅菌 輻射 第3部分:劑量測量指南》��、GB 18281.2-2015《醫(yī)療保健產(chǎn)品滅菌 生物指示物 第2部分:環(huán)氧乙烷滅菌用生物指示物》�、GB/T 19633.1-2015《最終滅菌醫(yī)療器械包裝 第1部分:材料、無菌屏障系統(tǒng)和包裝系統(tǒng)的要求》、GB/T 19633.2-2015《最終滅菌醫(yī)療器械包裝 第2部分:成形��、密封和裝配過程確認(rèn)的要求》���、YY/T 1267-2015《適用于環(huán)氧乙烷滅菌的醫(yī)療器械的材料評價》或者適用其他滅菌方式材料評價的標(biāo)準(zhǔn)�����、YY/T 0698系列標(biāo)準(zhǔn)等要求提交滅菌研究資料�����。
如果滅菌方式會導(dǎo)致有害物質(zhì)殘留�����,應(yīng)進(jìn)行相關(guān)評價��。如熱濕交換介質(zhì)等易吸附環(huán)氧乙烷���,環(huán)氧乙烷殘留量超標(biāo)會產(chǎn)生相應(yīng)危害。
3.2潔凈供應(yīng)的熱濕交換器微生物限度�����、環(huán)境及管理要求及檢查方法可結(jié)合申報產(chǎn)品的危險性程度和臨床使用最不利情況參照GB 15982-2012《醫(yī)院消毒衛(wèi)生標(biāo)準(zhǔn)》及《中華人民共和國藥典》提交研究資料。
4.效期和包裝研究
4.1產(chǎn)品有效期和包裝研究情況可通過實時老化或加速老化試驗獲得��。加速老化試驗可參照YY/T 0681和YY/T 0698系列標(biāo)準(zhǔn)����、GB/T 19633.1-2015《最終滅菌醫(yī)療器械包裝 第1部分:材料���、無菌屏障系統(tǒng)和包裝系統(tǒng)的要求》����、GB/T 19633.2-2015《最終滅菌醫(yī)療器械包裝 第2部分:成形��、密封和裝配過程的確認(rèn)的要求》�。使用的包裝材料為醫(yī)用級別。
4.2申請人應(yīng)提交包裝研究資料��,依據(jù)有關(guān)國內(nèi)�、國際標(biāo)準(zhǔn)進(jìn)行(如GB/T 19633.1、GB/T 19633.2���、ISO 11607���、ASTM F2475、ASTM D4169等)對包裝進(jìn)行分析研究和評價。直接接觸產(chǎn)品的包裝材料的選擇應(yīng)至少考慮以下因素:包裝材料的物理化學(xué)性能��;包裝材料的毒理學(xué)特性�����;包裝材料與產(chǎn)品的適應(yīng)性�;包裝材料與成型和密封過程的適應(yīng)性;包裝材料與滅菌或潔凈控制過程的適應(yīng)性���;包裝材料所能提供的物理�、化學(xué)和微生物屏障保護(hù)�;包裝材料與使用者使用時的要求(如無菌開啟)的適應(yīng)性;包裝材料與標(biāo)簽系統(tǒng)的適應(yīng)性�����;包裝材料與貯存運輸過程的適應(yīng)性����。
(九)產(chǎn)品技術(shù)要求的主要性能指標(biāo)
擬定產(chǎn)品技術(shù)要求應(yīng)符合《醫(yī)療器械注冊管理辦法》和《醫(yī)療器械注冊申報資料要求和批準(zhǔn)證明文件格式》(國家食品藥品監(jiān)督管理總局公告2014年第43號)的相關(guān)規(guī)定,按照《醫(yī)療器械產(chǎn)品技術(shù)要求編寫指導(dǎo)原則》(國家食品藥品監(jiān)督管理總局通告2014年第9號)要求編寫����。
本條款給出熱濕交換器的產(chǎn)品基本技術(shù)性能指標(biāo)�����,但并未給出定量要求�����,企業(yè)可參考相應(yīng)的國家標(biāo)準(zhǔn)、行業(yè)標(biāo)準(zhǔn)�,如YY/T 0735.1-2009《麻醉和呼吸設(shè)備 濕化人體呼吸氣體的熱濕交換器(HME) 第1部分:用于最小潮氣量為250mL的HME》、YY/T 0735.2-2010《麻醉和呼吸設(shè)備 用于加濕人體呼吸氣體的熱濕交換器(HMEs) 第2部分:用于氣管切開術(shù)患者的250mL以上潮氣量的HMEs》�����,根據(jù)企業(yè)自身產(chǎn)品的技術(shù)特點制定相應(yīng)的技術(shù)要求����。產(chǎn)品技術(shù)要求不得低于YY/T 0735.1-2009、YY/T 0735.2-2010等適用的相應(yīng)國家/行業(yè)標(biāo)準(zhǔn)要求�����。
1.物理性能
一般應(yīng)包括熱濕交換器患者端口接頭�����、附加端口(呼吸輔助裝置的接頭/呼吸附件接頭、輔助端口)�、水分損失(不同潮氣量的水分損失應(yīng)予以評價)、壓降�����、氣體泄漏��、順應(yīng)性�、外觀等。其中氣體泄漏���、順應(yīng)性不適用于連接氣管切開插管的熱濕交換器�����。
2.化學(xué)性能
根據(jù)不同材料特性�,由企業(yè)對化學(xué)性能提出要求���。用環(huán)氧乙烷滅菌的產(chǎn)品應(yīng)規(guī)定環(huán)氧乙烷殘留量的要求�����。
3.微生物要求
若以無菌形式提供�����,應(yīng)進(jìn)行無菌檢驗��。
非無菌供應(yīng)一次性使用的產(chǎn)品��,若產(chǎn)品使用前不需要進(jìn)行消毒����、滅菌處理,應(yīng)對其微生物限度進(jìn)行評價�����,同時可參考《中華人民共和國藥典》中微生物限度檢查法進(jìn)行檢測�。
4.若產(chǎn)品包含其他附加功能(如過濾性能)��,應(yīng)結(jié)合產(chǎn)品功能����、結(jié)構(gòu)制定相關(guān)性能要求。
(十)同一注冊單元內(nèi)注冊檢驗典型性產(chǎn)品確定原則
1.同一注冊單元中的典型產(chǎn)品是指能夠代表本注冊單元內(nèi)其他產(chǎn)品安全性和有效性的產(chǎn)品�����。其功能最齊全、結(jié)構(gòu)最復(fù)雜����、風(fēng)險最高。
2.典型產(chǎn)品的確定可以通過比較同一注冊單元內(nèi)所有產(chǎn)品的技術(shù)結(jié)構(gòu)�����、性能指標(biāo)和預(yù)期用途等相應(yīng)資料�����,說明其能夠代表本注冊單元內(nèi)其他產(chǎn)品的安全性和有效性�。若一個型號不能覆蓋,除選擇典型型號進(jìn)行全性能檢驗外�����,還應(yīng)選擇其他型號進(jìn)行差異性檢驗���。不同材料的熱濕交換介質(zhì)�����、不同型號規(guī)格(成人�����、兒童等)需要差異性檢驗�����。
同一規(guī)格型號的產(chǎn)品檢驗時“水分損失”���、“壓降”應(yīng)覆蓋不同潮氣量�����、氣體流量�。
(十一)產(chǎn)品生產(chǎn)制造相關(guān)要求
1.應(yīng)提供原材料質(zhì)控信息����,包括但不限于:原材料來源�、供應(yīng)商信息、原材料規(guī)范化學(xué)名稱/牌號�、安全性數(shù)據(jù)/化學(xué)品安全說明書、原材料符合標(biāo)準(zhǔn)/藥典/醫(yī)用級證明���、成分分析報告/檢驗報告/接受準(zhǔn)則�����。
2.應(yīng)當(dāng)明確熱濕交換器生產(chǎn)工藝流程����,注明關(guān)鍵工序和特殊過程,并說明其過程控制點�。
3.有多個研制、生產(chǎn)場地�,應(yīng)當(dāng)概述每個研制、生產(chǎn)場地的實際情況�����,相關(guān)的生產(chǎn)環(huán)境應(yīng)符合《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》(國家食品藥品監(jiān)督管理總局公告2014年第64號)的相關(guān)要求��。
4.詳細(xì)說明產(chǎn)品生產(chǎn)工藝過程及其確定的依據(jù)�����、質(zhì)量控制標(biāo)準(zhǔn)及其可靠性論證���;確認(rèn)關(guān)鍵工藝點并闡明其對產(chǎn)品物理性能�����、化學(xué)性能��、生物性能的影響�;確認(rèn)生產(chǎn)工藝的穩(wěn)定性。
5.對生產(chǎn)加工過程中所使用的所有輔劑���、助劑�����、粘合劑等添加劑均應(yīng)說明使用劑量��,提交對殘留量�、可揮發(fā)物質(zhì)總量的控制措施和接受標(biāo)準(zhǔn)以及安全性驗證報告��。例如鄰苯二甲酸酯等應(yīng)有限量要求�����。
(十二)產(chǎn)品的臨床評價要求
按照《醫(yī)療器械臨床評價技術(shù)指導(dǎo)原則》(國家食品藥品監(jiān)督管理總局通告2015年第14號)及《醫(yī)療器械注冊管理辦法》(國家食品藥品監(jiān)督管理總局令第4號)提交臨床評價資料��。
與《免于進(jìn)行臨床試驗醫(yī)療器械目錄》(國家藥品監(jiān)督管理局通告2018年第94號�,以下簡稱《目錄》)中,序號為345“一次性使用熱濕交換器/過濾器”相同的產(chǎn)品可免于進(jìn)行臨床試驗��。申請人需提交申報產(chǎn)品相關(guān)信息與《目錄》所述內(nèi)容的對比資料和申報產(chǎn)品與已獲準(zhǔn)境內(nèi)注冊的《目錄》中醫(yī)療器械的對比說明���。
若無法證明申報產(chǎn)品與《目錄》產(chǎn)品具有等同性��,則應(yīng)按照《醫(yī)療器械臨床評價技術(shù)審查指導(dǎo)原則》其他路徑開展相應(yīng)工作��,提供符合要求的臨床評價資料����。
(十三)產(chǎn)品的不良事件歷史記錄
企業(yè)應(yīng)提供相關(guān)信息����。
(十四)產(chǎn)品說明書和標(biāo)簽要求
產(chǎn)品說明書、標(biāo)簽和包裝標(biāo)識的編寫要求應(yīng)符合《醫(yī)療器械說明書和標(biāo)簽管理規(guī)定》(國家食品藥品監(jiān)督管理總局令第6號)和YY/T 0466.1-2016《醫(yī)療器械用于醫(yī)療器械標(biāo)簽�、標(biāo)記和提供信息的符號 第1部分:通用要求》的要求。同時應(yīng)注意以下要求:
1.使用前��,應(yīng)檢查產(chǎn)品是否完好�,如有破損禁止使用。
2.打開包裝�,檢查包裝內(nèi)器械是否完好無損。
3.將本產(chǎn)品病人端與通氣類器械連接����,另一端連接呼吸管路(連接氣管切開插管的熱濕交換器用于完全自主呼吸患者�����,不用連接呼吸設(shè)備)��,盡量靠近患者��。
4.具有吸痰孔的連接氣管切開插管的熱濕交換器可通過吸痰孔進(jìn)行定期吸痰���。
5.廢棄產(chǎn)品應(yīng)根據(jù)醫(yī)院或當(dāng)?shù)匦l(wèi)生主管部門的相關(guān)規(guī)定,由有資質(zhì)或經(jīng)授權(quán)的機(jī)構(gòu)進(jìn)行無害化處理�����。
6.僅限專業(yè)人員使用�����,使用時嚴(yán)格按照操作規(guī)程要求進(jìn)行����。
7.使用過程中應(yīng)加強(qiáng)呼吸道管理和監(jiān)測,監(jiān)測呼吸節(jié)律�����、頻率�����、血氧飽和度及心率�����,警惕缺氧和窒息表現(xiàn)����。出現(xiàn)異常時,應(yīng)檢查熱濕交換器是否通暢���,阻塞時應(yīng)及時更換����,或根據(jù)病人病情依照醫(yī)院制定的應(yīng)急預(yù)案進(jìn)行處理���。
8.使用過程中還需密切關(guān)注患者呼吸道情況����,一旦發(fā)現(xiàn)痰液黏稠或結(jié)痂的情況,就要采取主動加濕或其他措施�����。
9.預(yù)期與呼吸管路��、吸痰管�、吸氧管等配合使用,必須保證配合使用的器械滿足標(biāo)準(zhǔn)接口要求����。
10.使用無氣囊的氣管插管或氣管切開插管,插管周圍有漏氣現(xiàn)象會降低加濕效果���。
11.切勿給熱濕交換器添加水分��。
12.防止壓降不可接受的增加�。
13.使用過程中壓降會發(fā)生變化�,連接氣管切開插管的熱濕交換器通氧量會發(fā)生變化。
14.如產(chǎn)品中含有鄰苯二甲酸酯��,應(yīng)提示對兒童的風(fēng)險���,包括處于妊娠中的嬰兒或哺乳期女性�����。
15.提供的信息可包括接頭標(biāo)準(zhǔn)��、重量���、內(nèi)部容積、最長推薦使用時間�����,其他信息可參照YY/T0735.1或者YY/T0735.2第7章的要求�。
16.如發(fā)生過敏,應(yīng)立即停止使用�,并及時采取相應(yīng)的處置措施。
三�����、審查關(guān)注點
(一)重點關(guān)注產(chǎn)品技術(shù)要求編寫的規(guī)范性�,引用標(biāo)準(zhǔn)的適用性、準(zhǔn)確性����、有效性�����,是否結(jié)合產(chǎn)品的結(jié)構(gòu)制定相應(yīng)的性能指標(biāo)�。性能指標(biāo)的確定能否滿足產(chǎn)品的安全有效�。
(二)重點關(guān)注注冊申請人的產(chǎn)品研究資料是否全面、準(zhǔn)確���,是否體現(xiàn)其安全性�����、有效性��。
(三)臨床評價資料是否符合《醫(yī)療器械臨床評價技術(shù)指導(dǎo)原則》的要求�。
(四)產(chǎn)品檢驗報告:應(yīng)關(guān)注檢測的典型型號是否覆蓋所有性能要求���,檢驗報告所附照片中的產(chǎn)品結(jié)構(gòu)組成�����、標(biāo)識標(biāo)簽等信息��,是否與其他申報資料描述相同�。
(五)該產(chǎn)品若采用環(huán)氧乙烷滅菌,關(guān)注環(huán)氧乙烷殘留量�。
(六)若聲稱產(chǎn)品具有過濾功能,產(chǎn)品技術(shù)要求中應(yīng)制定相關(guān)性能要求���。
四�、編寫單位
河北省醫(yī)療器械與藥品包裝材料檢驗研究院
參與單位:
廣東省食品藥品監(jiān)督管理局審評認(rèn)證中心
河南省食品藥品審評查驗中心
內(nèi)蒙古自治區(qū)食品藥品審評查驗中心