醫(yī)療器械標簽標識盡管簡單����,但因為及其重要�,也最直觀,也是最容易被監(jiān)管到的錯誤事項�,因此,了解并正常使用符合MDR法規(guī)的標簽標識����,對醫(yī)療器械CE認證?企業(yè)來說非常重要。
醫(yī)療器械標簽標識盡管簡單����,但因為及其重要,也最直觀����,也是最容易被監(jiān)管到的錯誤事項,因此���,了解并正常使用符合MDR法規(guī)的標簽標識�����,對醫(yī)療器械CE認證企業(yè)來說非常重要�����。
與 MDD指令( 93/42/EEC )相比��, MDR的標簽需要更多信息�����,因為設備安全性和臨床有效性數(shù)據(jù)需要與用戶(醫(yī)務人員和患者/最終用戶)透明共享)��。歐盟 MDR附件 I 第 III 章“一般安全和性能要求”中涵蓋了有關(guān)隨醫(yī)療器械提供的信息的所有要求���。根據(jù)歐盟醫(yī)療器械法規(guī) (MDR)(第 2 條)中的定義���,“標簽”是指出現(xiàn)在器械本身、每個單元的包裝上或產(chǎn)品包裝上的任何書面��、印刷或圖形信息����。多個設備�����。貼標簽過程的目的是識別醫(yī)療器械及其制造商����,并傳達有關(guān)安全��、使用和性能的基本信息�����。它適用于醫(yī)療設備的用戶���,包括專業(yè)人士和消費者,以及相關(guān)第三方���。

醫(yī)療器械CE認證標簽����,一是確保涵蓋所有必要的符號和信息�����。另一個是標簽的大小。由于需要更多的符號和數(shù)據(jù)����,最大的挑戰(zhàn)將是如何將它們?nèi)糠旁跇撕炆稀T跇撕炘O計過程中�,請記住以下幾點:標簽和說明的媒介、格式�����、內(nèi)容�����、易讀性和位置必須與預期用戶的技術(shù)知識���、經(jīng)驗�、教育或培訓相匹配�����。此外��,使用說明必須以預期用戶易于理解的術(shù)語編寫�,并在適當?shù)那闆r下補充附圖和圖表���。標簽可以以人類可讀的格式提供,并且可以用機器可讀的信息來補充�����。
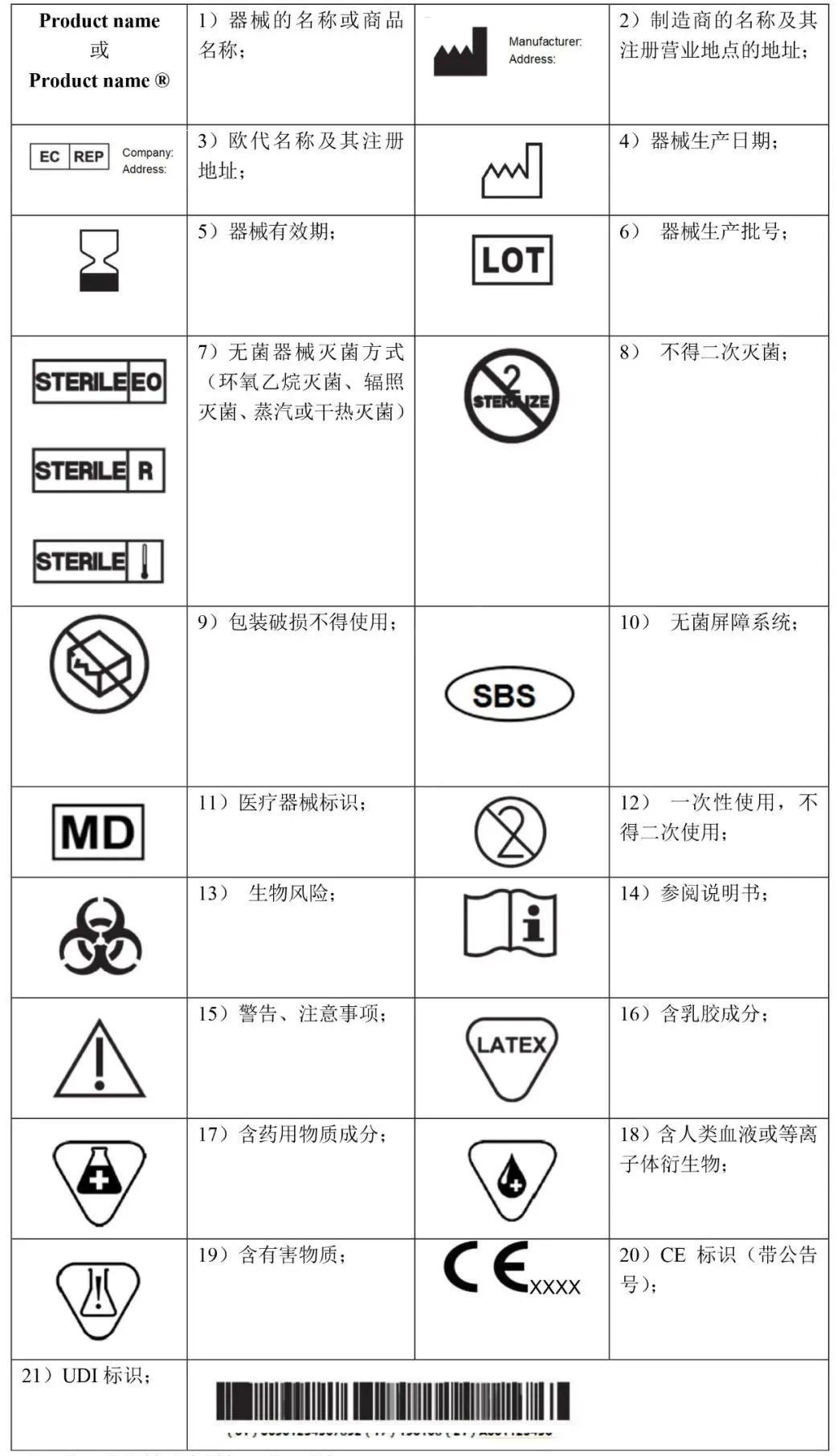
如下是常見標識�。
任何有關(guān)醫(yī)療器械CE認證的需求,歡迎您隨時方便與杭州證標客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡��!