適用于動靜脈瘺的建立的人工血管在我國屬于第三類醫(yī)療器械注冊產(chǎn)品�����,該產(chǎn)品為多層結(jié)構(gòu)����,在膨體聚四氟乙烯(ePTFE)內(nèi)層 和聚對苯二甲酸乙二醇酯(PET)編結(jié)物外層之間,有加強型聚丙烯(PP)支撐環(huán)和硅膠層�����。環(huán)氧乙烷滅菌����,一次性使用。本文為大家介紹人工血管產(chǎn)品技術(shù)要求及注冊審評要點�����,一起看正文�。
適用于動靜脈瘺的建立的人工血管在我國屬于第三類醫(yī)療器械注冊產(chǎn)品,該產(chǎn)品為多層結(jié)構(gòu)�,在膨體聚四氟乙烯(ePTFE)內(nèi)層
和聚對苯二甲酸乙二醇酯(PET)編結(jié)物外層之間,有加強型聚丙烯(PP)支撐環(huán)和硅膠層��。環(huán)氧乙烷滅菌,一次性使用�����。本文為大家介紹人工血管產(chǎn)品技術(shù)要求及注冊審評要點�����,一起看正文����。
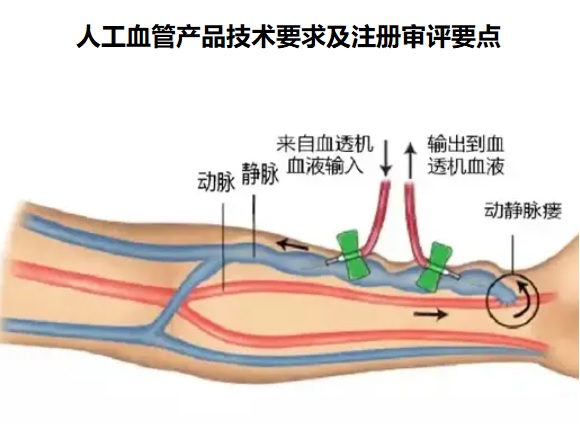
一、人工血管的工作原理
人工血管是一種非來源于自然器官和組織的血管代用
品���,人工血管可用于血液透析患者的動靜脈通路建立�����,在血
液通路手術(shù)中作為皮下動靜脈通路。
二�、人工血管產(chǎn)品技術(shù)要求
人工血管產(chǎn)品技術(shù)要求中的性能指標通常用包括:外觀、自然狀態(tài)下內(nèi)徑��、有效長度�����、壁厚、水滲透壓�����、軸向拉伸強度��、圓周拉伸強度��、探針破裂強度�����、牽拉強度���、反復穿刺后圓周拉伸強度���、扭結(jié)半徑、擴張內(nèi)徑�����、動態(tài)順應性�����、微粒污染、單位面積重量�����、還原物質(zhì)����、蒸發(fā)殘渣、紫外吸光度����、酸堿度、重金屬總量�、環(huán)氧乙烷殘留量、六甲基二硅氧烷殘留量�、無菌、細菌內(nèi)毒素這24項性能指標�。
三、人工血管產(chǎn)品注冊時����,生物相容性試驗應開展哪幾項����?
人工血管為植入器械�,與人體循環(huán)血液長期接觸��。醫(yī)療器械注冊申請人依據(jù) GB/T 16886 系列標準進行了生物相容性評價��,選擇了材料表征����、毒理學評價和生物學試驗的方式進行風險評定,開展的生物學試驗包括溶血���、血栓形成���、凝血、熱原�����、急性全身毒性�、細胞毒性、致敏��、皮內(nèi)反應、植入后局部組織反應��、遺傳毒性�����、亞慢性全身毒性��;針對亞急性毒性����、慢性毒性、致癌性終點開展了評價�����。
如有人工血管產(chǎn)品注冊咨詢服務需求����,或是其他第三類醫(yī)療器械注冊代理服務需求,歡迎您隨時方便與杭州證標客醫(yī)藥技術(shù)咨詢有限公司聯(lián)絡��,聯(lián)系人:葉工��,電話:18058734169���,微信同�����。